Chlamydiose
Historique
Plus connu chez l'Homme sous le terme d'ornithose psittacose, la chlamydiose est une infection bactérienne liée à Chlamydophila psittaci.
Les connaissances sur la bactérie, son épidémiologie, son pouvoir pathogène ont été en très grande partie acquises en 1929, suite à un épisode de contamination humaine lié à l'importation d'oiseaux exotiques contaminés d'Argentine vers l'Europe et les Etats Unis. Plus de 1000 cas de pneumonie ont alors été recensés conduisant dans 20 à 30 % des cas à la mort des malades. Cette maladie est aujourd'hui mondialement répandue.
On a longtemps cru que cette maladie touchait uniquement les oiseaux exotiques et plus particulièrement les psittacidés, mais aujourd'hui différents travaux montrent que les volailles de rente peuvent également représenter un réservoir d'infection non négligeable.
La chlamydiose à C. psittaci représente la forme de chlamydiose animale transmissible à l'homme la plus importante. Cette synthèse bibliographique a pour objet de décrire la chlamydiose aviaire et d'évoquer les mesures de prévention qui peuvent être prises en terme de santé publique.
Origine de la maladie
La chlamydiose est causée par une bactérie : Chlamydophila psittaci. Une classification récente au sein de la famille des chlamydiaceae a séparé les Chlamydia (C. trachomatis, C. suis) des Chlamydophila. Au sein des C. psittaci, l'espèce responsable d'avortements chez les bovins et les petits ruminants est désormais baptisée C. abortus. Cette nouvelle taxonomie date de travaux menés en 1999 par Everett et Coll et est basée sur l'analyse des gènes codant pour les ARN 16S et 23S.
C. psittaci est une bactérie intracellulaire, gram négative, immobile d'un diamètre de 0,2 à 1, 5 µm. Il existe 6 variétés (serovars) de chlamydophila psittaci toutes détectées par la technique utilisée à LABOFARM.
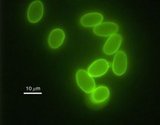
Elle se développe dans des vacuoles selon un cycle particulier au cours duquel le corps élémentaire (forme infectieuse) après pénétration dans la cellule hôte passe par un état de corps réticulé puis de corps intermédiaire qui, après maturation se transforme à nouveau en corps élémentaire, relargués par lyse cellulaire ou division de la cellule hôte. Cette forme infectieuse est relativement peu résistante dans l'environnement et sensible aux désinfectants.
Si à l'origine on pensait que C. psittaci ne concernait que les becs crochus, de nombreuses études ont depuis montré que la bactérie était présente chez plus de 450 espèces d'oiseaux incluant 17 genres différents : ainsi l'ordre des Passériformes, des Colombiformes, des Galliformes, des Ansériformes... Dans les années 30, dans les Iles Féroé, des cas de pneumonies humaines létales ont été observés suite à l'infection par des fulmars boréals (Fulmarus glacialis).
Plusieurs travaux ont montré le lien étroit pouvant exister entre la pneumonie développée par un éleveur et le portage de C. psittaci par ses propres oiseaux. En effet certaines souches très virulentes ne nécessitent qu'un contact très fugace entre l'Homme et l'oiseau pour installer une infection efficace.
Signes cliniques
Chez l 'Homme, on observe plusieurs dizaines de cas par an en France principalement chez les éleveurs et ramasseurs de volailles (canards notamment), les éleveurs d'oiseaux, le personnel des parcs zoologiques et des animaleries, les salariés des abattoirs et le personnel des laboratoires d'analyses,
La maladie se transmet généralement par inhalation de poussières ou de fientes contaminées.
Les symptômes peuvent se manifester sous 3 formes possibles :
- Une conjonctivite avec maux de tête importants après quelques jours d'incubation.
- Une forme respiratoire après incubation de 5 à 15 jours ressemblant à une forte grippe (39 à 40° C), frissons, douleurs musculaires, toux, pneumonie, grande fatigue, convalescence souvent lente, complications cardiaques possibles...
- Une forme généralisée, septicémique, très grave avec complications respiratoires, digestives (diarrhées), neurologiques(troubles de la conscience, méningite, encéphalite,,,), cardiaques, rénales...
La mortalité qui peut atteindre 10 à 20% des malades en absence de traitement, est inférieure à 1% si la maladie est traitée à temps avec un traitement antibiotique approprié.
Chez les oiseaux dans une grande partie des cas, les oiseaux peuvent manifester aucuns symptômes (forme silencieuse de la maladie- porteurs asymptômatiques-).
En 1989 deux chercheurs néerlandais, les Dr Van Burren et Gerry Dorrestein, estimaient que 40 % des élevages de perruches ondulées de leur pays étaient porteurs inapparents de Chamydophila psittaci.
Des études effectuées sur les pigeons des grandes villes françaises mettent en évidence la présence de la bactérie chez une grande majorité (50 à 70%) de sujets ne montrant aucun signe de maladie.
En cas de symptômes la maladie peut se manifester sous trois formes :
Une forme suraiguë :
Mort rapide sans signes préalables, le plus souvent chez de très jeunes oiseaux ou sur les petits exotiques.
Une forme aiguë :
Visible en particulier chez les grands perroquets (Aras, Amazones, Gris du Gabon...), les sujets se mettent « en boule », sont abattus, fiévreux, amaigris, présentent des écoulements oculaires et des écoulements au niveau des narines, des conjonctivites, des troubles respiratoires et des troubles nerveux qui précèdent en général la mort de l'animal...
Une forme chronique :
Elle se traduit par différents aspects (difficultés respiratoires : toux, éternuements, jetage nasal ; amaigrissement ; troubles de la reproduction (baisse de fertilité, d'éclosabilité et mortalité accrue chez les jeunes...), quelques fois troubles nerveux (torticolis, convulsions, tremblements...).
Souvent, les patients atteints de la forme chronique semblent apparemment guérir mais deviennent porteurs asymptomatiques, excréteurs temporaires de la bactérie.
Voies de contamination
La principale voie de contamination est la voie respiratoire. La bactérie est présente chez les oiseaux malades ou asymptomatiques sur les plumes, dans les sécrétions nasales et oculaires et dans les fientes. La contamination se fait donc par inhalation de particules infectées. Une contamination par contact direct entre oiseaux ou indirect via le matériel d'élevage (mangeoire, accessoires dans les volières...) est également possible L'excrétion de C. psittaci chez les oiseaux asymptomatiques est intermittente, ce qui rend d'autant plus difficile leur détection dans les fientes. Cette excrétion peut être réactivée par un stress environnemental (changement de propriétaire...) ou physiologique (entrée en reproduction).
D'autre part, il semblerait que selon l'ancienneté de l'infection, la bactérie se retrouve plus facilement au niveau de la sphère respiratoire (infection récente) ou au niveau cloacal et fécal (infection ancienne).
La bactérie, quoique peu résistante dans l'environnement sous la forme de corps élémentaire seul, peut cependant conserver plusieurs mois un caractère infectieux si elle est protégée par des matières organiques (litière, fientes...)
Diagnostic
Du fait de la faible résistance de la bactérie dans le milieu extérieur, il n'est pas utile de la rechercher dans l'environnement. Le dépistage de C. psittaci sera donc mené sur l'oiseau lui-même.
A l'examen, les lésions sont à peu près les mêmes chez tous les oiseaux. Leur importance est liée à l'ancienneté de la maladie. Les lésions respiratoires sont représentées par une atteinte des sacs aériens (opacification, épaississement, œdème), des poumons œdémateux (œdème généralisé ou zonaire), un dépôt fibrineux sur plusieurs organes (péricarde, foie, intestin), un foie marbré ou hémorragique, hypertrophié. Chez les psittacidés, la lésion la plus caractéristique et parfois unique, est une hypertrophie de la rate. L'atteinte intestinale signe une infection aiguë et le contenu est vert-jaune, gélatineux à liquide.
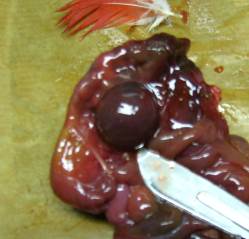
Splénomégalie (hypertrophie de la rate)
Sur Gris du Gabon âgé de deux ans
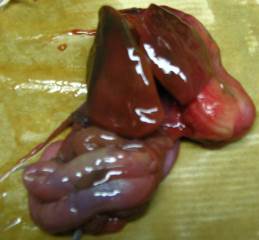
Hépatite
La culture bactérienne , du fait du caractère intracellulaire de Chlamydophila psittaci est longue et délicate et n'est réalisée que dans des laboratoires très spécialisés.
La mise en évidence du germe par la technique PCR (Polymerase Chain Reaction) est aujourd'hui la méthode la plus utilisée en médecine humaine et vétérinaire.
La spécificité et la sensibilité de la méthode en font un outil performant notamment pour les animaux porteurs de la maladie sans signes apparents (porteurs asymptomatiques) et excréteurs de la bactérie à un faible niveau.
Sur un sujet mort le diagnostic s'effectuera à partir d'un prélèvement d'organe lésé (mélange foie + rate le plus généralement).
Sur un sujet vivant présentant des symptômes respiratoire la recherche pourra s'effectuer à partir d'un écouvillon de secrétion oculaire ou nasal + écouvillon de cloaque ( Labofarm fourni les écouvillons stériles sur demande).


Sur un sujet vivant ne présentant pas de symptômes le prélèvement de choix reste l'écouvillon de cloaque ou à défaut un échantillon de fientes récoltées sur 3 à 4 jours.
Remarque :
il est complètement illusoire de vouloir dépister la présence de Chlamydia psittaci à partir d'un prélèvement sanguin si l'animal ne présente pas de symptômes voire même s'il n'est pas en phase terminale de la maladie.
Traitement & vaccination
Il n'existe pas à ce jour de vaccin contre la chlamydiose.
Les antibiotiques sont généralement efficaces sur Chlamydophila psittaci si l'affection est prise à temps et si le traitement est administré suffisamment longtemps (sur 5 à 7 semaines).
Les molécules les plus couramment utilisées sont les dérivés des tétracyclines (Oxytétracycline, Doxycycline -Ronaxan®- , Chlortetracycline.... Et les quinolones (enrofloxacine- Baytril®-).
Dans tous les cas prenez contact avec votre vétérinaire pour mettre en place un protocole de traitement adapté à votre élevage et à l'espèce concernée.
En résumé :
La chlamydiose est une zoonose (maladie pouvant être transmise à l'homme) qui peut être très grave notamment chez les jeunes enfants, les personnes âgées et les personnes souffrant d'une maladie chronique...).
En cas de troubles respiratoires persistants (signes grippaux, toux...) n'hésitez pas à signaler à votre médecin traitant que vous vivez en contact avec un perroquet ou tout autre oiseau d'ornement.
La maladie se transmet par contact buccal ou par inhalation de poussières de fientes contaminées.
La méthode la plus fiable pour diagnostiquer ou dépister la maladie est le test PCR développé par LABOFARM .
Les prélèvements recommandés sont le foie et la rate en cas de diagnostic sur animal mort, un écouvillon de cloaque + écouvillon d'écoulement oculaire et nasal chez un oiseau présentant des troubles respiratoires, un écouvillon de cloaque chez l'animal qui ne présente pas de signes apparents.
Les tests réalisés à partir d'un prélèvement de sang ne sont pas satisfaisants (risque important de faux négatifs).
Il n'existe pas de vaccin. Les traitements antibiotiques (tétracyclines et quinolones) sont efficaces vis-à-vis de la maladie s'ils sont administrés suffisamment longtemps, à la bonne posologie, et s'ils sont associés à des mesures d'hygiène et de prévention strictes (quarantaine, désinfection...)
En cas de tests positifs consultez votre vétérinaire pour établir un protocole de traitement approprié.
Références
- Andersen AA, 1996, Comparison of pharyngeal, fecal, and cloacal samples for the isolation of Chlamydia psittaci from experimentally infected cockatiels and turkeys, J Vet Diagn Invest, 8:448-450.
- Olsen B, Persson K, Broholm KA, 1998, PCR Detection of Chlamydia psittaci in faecal samples from passerine birds in Sweden, Epidemiol Infect, 121: 481-483.
- J.P. André 2004 Oiseaux de cages et de volières- de la maladie à la bonne santé
- Document Ornithose-Psittacose du ministère de l'agriculture et de la pêche, DGFAR, DGAL 2006
- www.avma.org/pubhlth/psittacosis.asp
- Léon O, Sraka B, Guérin JL, mai 2005, Les infections à Chlamydophila psittaci chez les volailles et leur impact en santé publique, Bulletin des GTV, 239-244.
P. Lamandé
Responsable service Oiseaux d'ornement LABOFARM.






